Перейти к:
Применение метода капилляроскопии ногтевого ложа с целью оценки эффективности проводимой терапии (дупилумаб) у пациента с тяжелой бронхиальной астмой
https://doi.org/10.31146/2949-4664-apps-3-2-58-65
Аннотация
Бронхиальная астма остается одной из актуальных проблем современного здравоохранения ввиду высокой распространенности, роста заболеваемости, серьезного экономического бремени. Своевременная диагностика, определение предикторов развития заболевания, а также оценка эффективности терапии являются ключевыми факторами раннего выявления, предотвращения прогрессирования астмы, уменьшения риска осложнений, разработки персонифицированного лечения, что способствует улучшению качества жизни пациентов. Нами на клиническом примере была продемонстрирована перспективность и практическая значимость применения метода визуализации сосудов микроциркуляции для диагностики заболевания, а также оценки эффективности проводимой биологической терапии (дупилумаб) у пациента, страдающего тяжелой бронхиальной астмой.
Ключевые слова
Для цитирования:
Бережанский П.А., Хургаева А.Э., Малахов А.Б., Гутырчик Т.А., Шаталина С.И., Колосова Н.Г. Применение метода капилляроскопии ногтевого ложа с целью оценки эффективности проводимой терапии (дупилумаб) у пациента с тяжелой бронхиальной астмой. Архив педиатрии и детской хирургии. 2025;3(2):58-65. https://doi.org/10.31146/2949-4664-apps-3-2-58-65
For citation:
Berezhanskiy P.V., Khurgaeva A.E., Malakhov A.B., Gutyrchik T.A., Shatalina S.I., Kolosova N.G. Using nailfold capillaroscopy to assess the effectiveness of ongoing therapy (dupilumab) in a patient with severe bronchial asthma. Archives of Pediatrics and Pediatric Surgery. 2025;3(2):58-65. (In Russ.) https://doi.org/10.31146/2949-4664-apps-3-2-58-65
Введение
Бронхиальная астма (БА) представляет собой полиэтиологическое заболевание со сложным патогенезом, в основе которого лежит хроническое воспаление дыхательных путей, сопровождающееся ограничением воздушного потока на выдохе и характеризующееся такими респираторными симптомами, как одышка, затрудненное дыхание, кашель и свистящие хрипы [1].
В руководствах Глобальной инициативы по бронхиальной астме (Global Initiative for Asthma — GINA), а также в Федеральных клинических рекомендациях по БА выделяют фенотипы в зависимости от демографических, клинических и патофизиологических характеристик: аллергическая, неаллергическая, бронхиальная астма с поздним дебютом, с фиксированной обструкцией и связанная с ожирением [1][2]. Однако данная классификация не учитывает основные биологические механизмы, участвующие в формирования заболевания и являющиеся основными мишенями для терапии. В связи с этим было предложено в дополнение к фенотипам группировать БА на эндотипы в зависимости от ведущих механизмов воспаления: Т2-эндотип (в основе лежит аллергическое воспаление с участием клеток Т2-иммунного ответа (Th2-клетки и врожденные лимфоидные клетки 2-го типа) и интерлейкинов (IL-4, -5, -13 и др.)) и не Т2-эндотип (ведущую роль играют нейтрофилы и паугранулоцитарные клетки, а также выделяемые ими биологически активные молекулы (IL-6, -8, 17А/F)) [3].
В основе верификации диагноза БА лежит комплексный подход, включающий сбор жалоб, анамнеза, совокупность лабораторных (гемограмма, определение общего IgE и специфических IgE в сыворотке крови) и инструментальных методов обследования (спирометрия, пикфлоуметрия, бодиплетизмография, исследование уровня оксида азота в выдыхаемом воздухе и др.) [2]. К одному из современных перспективных методов диагностики БА также следует отнести исследование сосудов микроциркуляторного русла с помощью компьютерной капилляроскопии ногтевого ложа. Данный инновационный метод имеет множество преимуществ: позволяет оценить состояние капилляров в режиме реального времени, является неинвазивным и безболезненным, не имеет возрастных ограничений, а также не требует специальных условий проведения [4][5].
Доказано, что в развитии БА одно из значимых влияний оказывает изменение сосудов микроциркуляторного русла [6]. Развивающиеся обструктивные нарушения и, как следствие, гипоксия у пациентов с астмой приводят к нарастающим морфофункциональным изменениям всех клеточных структур легких, в том числе легочной паренхимы и сосудов, приводящих к гемодинамическим нарушениям со снижением эффективного функционирования дыхательной системы [7]. Изменения микроциркуляции в дыхательной системе являются критическими факторами патофизиологических нарушений при БА, сопровождающими ее развитие и течение. При этом степень их выраженности определяет прогноз заболевания, что имеет практическое значение для поиска ранних признаков адаптированности гемодинамики к начальным изменениям бронхиальной проходимости в начальной стадии развития БА (с целью ранней диагностики и профилактики заболевания), верификации диагноза, а также динамического наблюдения для оценки эффективности проводимой терапии [8][9].
Считается, что капиллярная сеть у пациентов с аллергическими заболеваниями (в том числе у пациентов, страдающих БА) имеет морфологические различия («клубочкообразную» и «древовидную» формы концевых капилляров), измененную архитектонику, увеличение количества капилляров на единицу площади, недостаточную дифференцировку капилляров на уровне 3-го порядка, замедление кровотока и изменение капилляроскопических параметров сосудов микроциркуляторного русла. Все это является следствием перегрузки сосудов в результате компенсаторных механизмов, вызванных гипоксией, влиянием медиаторов воспаления, а также ингибированием апоптоза эндотелиоцитов и факторов ангиогенеза [4][10]. При этом выявляемые нарушения капилляров в острую фазу аллергического воспаления может наблюдаться на этапе доклинических проявлений заболевания, что может использоваться как один из предикторов риска развития БА [11].
Например, в проведенном наблюдательном исследовании в условиях поликлиники было обследовано 150 детей с отягощенным аллергоанамнезом, где на основании полученных данных был проведен факторный и кластерный анализ, при помощи которого удалось определить наиболее значимые прогностические показатели изменений микроциркуляторного русла, характерные для детей с высоким риском развития БА: увеличение диаметра венулярной части капилляров, снижение скорости капиллярного кровотока, увеличение количества функционирующих капилляров на единицу площади. В катамнезе в течение 5 лет у 30% пациентов была диагностирована бронхиальная астма [12].
Таким образом, дисфункция микроциркуляторного русла является ключевым звеном патогенеза при БА, а применение метода компьютерной капилляроскопии, позволяющий объективно оценить состояние капилляров, имеет большое значение для определения тактики ведения пациентов [10][12].
Известно, что главным фактором в рациональном ведении пациентов с БА после верификации диагноза является назначение эффективного лечения. Более 30 лет в терапии БА основную роль играет использование глюкокортикостероидов (ГКС), которые уменьшают эозинофильное воспаление в дыхательных путях, купируют приступы и выраженность симптомов [13]. В Федеральных клинических рекомендациях Российской Федерации по ведению детей с БА, в национальной программе «Бронхиальная астма у детей», а также в согласительном документе GINA в лечении пациентов, страдающих БА, используется ступенчатая базисная терапия и препараты для купирования симптомов бронхообструкции [1][2][14]. Однако около 10% взрослых и 2,5% детей плохо переносят терапию ГКС и/или имеют тяжелую бронхиальную астму (ТБА), которая часто является резистентной к стандартной противовоспалительной терапии [13].
В 2021 г. в рекомендациях GINA определение ТБА было изменено. Если ранее оно соотносилось по ступеням терапии, то в настоящее время считается, что ТБА — астма, которая остается неконтролируемой, несмотря на оптимизированное лечение высокими дозами ингаляционных глюкокортикостероидов (ИГКС) или β2-агонистов длительного действия, или ухудшается при попытке снижения дозы ИГКС [1]. При этом ТБА имеет один или два признака: недостаточный контроль над симптомами; частые обострения (≥2 в течение года), требующие применения системных ГКС, или одно обострение, которое привело к госпитализации в течение года [1]. В России согласно Федеральным клиническим рекомендациям ТБА до инициации базисной терапии определяется на основании классификации, где учитывается количество дневных и ночных симптомов, влияние обострений на физическую активность, а также показатели функции внешнего дыхания [2]. Тяжелая астма является на сегодня не только медицинским, но и социальным бременем современного общества, так как пациенты с ТБА представляют собой группу высокого риска тяжелых жизнеугрожающих обострений (в том числе астматического статуса), приводящих к инвалидизации и смерти [15–17].
Принимая во внимание необходимость разработки новых методов лечения пациентов, страдающих ТБА и резистентных к стандартной противовоспалительной терапии, была создана таргетная терапия, основными мишенями которой являются звенья патогенеза воспаления при БА. Биологическая терапия произвела революцию в лечении БА в мире. Моноклональные антитела, действие которых основано на блокировании различных звеньев патогенеза воспаления, способствуют достижению контроля симптомов астмы, минимизации количества обострений, улучшению показателей внешнего дыхания, тем самым улучшая качество жизни пациентов [18].
На сегодня в Российской Федерации зарегистрировано шесть генно-инженерных биологических препаратов (ГИБП): омализумаб (анти-IgE антитела), дупилумаб (антитела к рецепторам к α-субъединицы IL-4), бенрализумаб (антагонист рецептора IL-5), меполизумаб и реслизумаб (антагонисты IL-5), тезепелумаб (ингибитор тимического стромального лимфопоэтина (TSLP)) [2] (рис. 1).
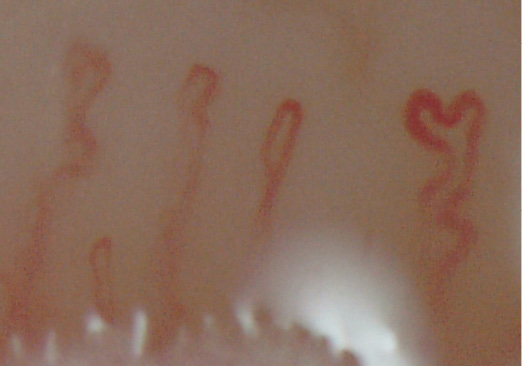
Рисунок 1.
Периваскулярный отек, измененные «древовидные» формы капиллярных петель (увеличение × 400)
Figure 1.
Perivascular edema, altered «tree-like» shapes of capillary loops (magnification × 400)

Рисунок 2.
Периваскулярный отек, измененные «древовидные» формы капиллярных петель (увеличение × 500)
Figure 2.
Perivascular edema, altered “tree-like” shapes of capillary loops (magnification × 500)
Дупилумаб представляет собой полностью гуманизированное моноклональное антитело (IgG4) к рецептору IL-4Rα, которое блокирует передачу сигнала от IL-4 и IL-13, являющихся ключевыми факторами Т2-воспаления [19]. В проведенном многонациональном многоцентровом рандомизированном двойном слепом плацебо-контролируемом исследовании (Liberty Asthma QUEST) была показана эффективность применения дупилумаба у пациентов, страдающих ТБА: снижение частоты тяжелых обострений в течение года и потребности в применении пероральных ГКС, а также улучшение показателей функции внешнего дыхания [20]. Препарат используется не только в лечении ТБА, в Российской Федерации также зарегистрирован опыт применения при атопическом дерматите, хроническом полипозном риносинусите, эозинофильном эзофагите [21].
Клиническое наблюдение
Пациент и его законные представители дали свое информированное согласие на обработку своих персональных данных.
Мальчик, 10 лет, поступил в отделение пульмонологии Морозовской детской клинической больницы 28.05.2024 г. с жалобами на периодически возникающие эпизоды затрудненного дыхания, свистящих хрипов, плохую переносимость физических нагрузок, кашель на фоне физических нагрузок.
Анамнез жизни: ребенок от первой беременности, протекавшей без особенностей, от первых срочных, самопроизвольных родов. Масса тела при рождении — 3400 г, длина тела — 51 см. Оценка по шкале APGAR — 9/10 баллов. На первом году жизни у ребенка наблюдались проявления атопического дерматита, с двух лет — аллергический ринит.
Семейный анамнез по аллергологическим заболеваниям отягощен: у матери — аллергический ринит.
Из анамнеза заболевания известно, что ребенок наблюдается с диагнозом «бронхиальная астма» с 2018 года. Получал с 5 лет базисную терапию: флутиказон + салметерол 25/125 мкг по 2 дозы 2 раза в сутки; в период обострения: ингаляции с ипратропия бромидомом + фенотерол и будесонидом. Несмотря на приверженность терапии и отсутствие сопутствующих заболеваний, бронхиальная астма оставалась неконтролируемой: ребенка беспокоили частые обострения, плохая переносимость физической нагрузки, возникала необходимость в госпитализациях. В 2024 году ребенок получал объем терапии, соответствующий четвертой ступени согласно GINA (будесонид + формотерол 80/4,5 мкг по 2 дозы 2 раза в сутки, тиотропия бромид 2,5 мкг/доза по 2 дозы 1 раз в сутки) (табл. 1).
Таблица 1.
Динамика показателей вентиляционной функции легких по данным спирометрии за период с 2018 по 2024 г.
Table 1.
Longitudinal changes in spirometry-based ventilatory pulmonary function: 2018–2024
Показатели вентиляционной функции легких по данным спирометрии (ОФВ1, ЖЕЛ и ОФВ1/ ЖЕЛ) | Проба с бронхолитиком (прирост ОФВ1) | |
2018 г. | норма | + 18% |
базисная терапия — флутиказон + салметерол | ||
2018 г. | норма | проба отрицательная |
2020 г. | обструкция легкой степени | + 19% (240 мл) |
2022 г. | выраженная обструкция | + 58% (750 мл) |
базисная терапия — будесонид + формотерол, тиотропия бромид | ||
2023 г. | обструкция легкой степени | + 21% (270 мл) |
2024 г. | обструкция легкой степени | + 26% (300 мл) |
Примечание: ОФВ1 — объем форсированного воздуха за 1 секунду, ЖЕЛ - жизненная емкость легких.
Note: FEV1 – forced expiratory volume in 1 second, VC – vital capacity.
По данным лабораторных исследований также было выявлено повышение общего IgE: в 2020 г. — 1206 МЕ/мл, в 2023 г. — 851 МЕ/мл; сенсибилизация к эпидермальным и пыльцевым аллергенам (береза, тимофеевка, домашняя пыль, кошка).
С 2022 года на фоне регулярной базисной терапии сохраняются вышеуказанные жалобы. При этом обострение бронхиальной астмы — несколько раз в месяц, два эпизода ночных пробуждений за последние 4 недели (купированы дополнительной ингаляцией будесонид + формотерол 80/4,5 мкг).
Объективный осмотр при поступлении:
Общее состояние — средней тяжести, ребенок в сознании. Кожные покровы обычной окраски, на коже верхних и нижних конечностей — единичные элементы папулезных высыпаний с очагами лихенификации (проявления атопического дерматита). Видимые слизистые розовые, чистые. Дыхательная система: частота дыхательных движений — 21 в минуту, при аускультации — дыхание жесткое, выслушиваются единичные сухие свистящие хрипы, одышки на момент осмотра нет, сатурация составляет 98%. Со стороны сердечно-сосудистой системы — без патологии. Живот при пальпации мягкий, безболезненный. Стул регулярный, мочеиспускание не нарушено.
Проведенное обследование в пульмонологическом отделении:
- рентгенография органов грудной клетки от 29.05.2024 г.: убедительных данных за наличие очаговых и инфильтративных изменений не выявлено;
- спирометрия от 30.05.2024 г.: нарушения вентиляционной функции легких по обструктивному типу тяжелой степени, ОФВ1— 60%. Тест с бронхолитиком (фенотерол 300 мкг через спейсер) резко положительный: по ОФВ1 + 58%, 760 мл;
- в клиническом анализе крови — эозинофилия 680 кл/мкл, остальные показатели без клинически выраженных отклонений; в биохимическом анализе — уровень С-реактивного белка (СРБ) отрицательный, в иммунологическом исследовании — повышенный уровень общего IgE— 949,00 МЕ/мл, sIgE к аллергенам кошки (3‑й класс), собаки (2‑й класс), деревьев (2‑й класс), клещам (1‑й класс);
- АСТ-тест — 17 баллов;
- капилляроскопия ногтевого ложа от 30.05.2024 г.: наблюдается выраженный отек периваскулярной зоны, измененные «древовидные» формы капиллярных петлей, значимое сужение артериальной части капилляров (рис. 1, 2).
На основании жалоб (эпизоды затрудненного дыхания, дистанционные свистящие хрипы, плохая переносимость физических нагрузок, кашель на фоне физических нагрузок), данных анамнеза заболевания (наблюдается с диагнозом БА с 5 лет, недостаточный контроль симптомов, частые обострения), отягощенного аллергологического анамнеза (атопический дерматит — на первом году жизни, аллергический ринит — с двух лет, отягощенный семейный анамнез по аллергическим заболеваниям), объективного осмотра (при аускультации — дыхание жесткое, выслушиваются единичные сухие свистящие хрипы), проведенной инструментальной (по данным спирометрии — признаки вентиляционных нарушений по обструктивному типу, данные капилляроскопии ногтевого ложа: периваскулярный отек, измененные «древовидные» формы капиллярных петлей) и лабораторной диагностики (эозинофилия в клиническом анализе крови, повышение уровня общего IgE, выявление специфических IgE), проведенной дифференциальной диагностики (с пневмонией — отсутствие инфильтративных изменений по данным рентгенографии, отсутствие лихорадки и повышения маркеров воспаления по лабораторным данным) у ребенка установлен диагноз: бронхиальная астма, атопическая форма, тяжелое течение, неконтролируемая, вне обострения, ДН 0 степени, с сенсибилизацией к эпидермальным и пыльцевым аллергенам. Сопутствующими заболеваниями являются атопический дерматит, легкое течение, ограниченно-локализованная форма, стадия неполной ремиссии; аллергический ринит в стадии ремиссии.
Принимая во внимание неконтролируемое течение бронхиальной астмы, недостаточный эффект от проводимой базисной терапии 4‑й ступени, явления атопического дерматита, ребенку была показана инициация иммунобиологической терапии ГИБП — дупилумаб в стартовой дозировке 400 мг, далее по 200 мг каждые 14 дней.
07.06.2024 г. курс стационарного обследования и лечения был завершен. Ребенок выписан из стационара с рекомендациями под наблюдение педиатра, пульмонолога, аллерголога-иммунолога по месту жительства.
Результаты терапии дупилумабом: ребенок каждые 14 дней получал ГИБП (дупилумаб), на фоне которой были отмечены улучшения: приступы бронхообструкции стали реже, ночные пробуждения не беспокоили, переносимость физической нагрузки стала лучше.
03.11.2024 г. при плановом амбулаторном осмотре мальчику было проведено обследование:
- АСТ-тест — 23 балла (частично контролируемое течение);
- спирометрия: показатели ФВД — в пределах возрастных норм, проба с бронхолитиком — отрицательная;
- капилляроскопия: капиллярные петли стали менее извитыми, имели правильную форму шпильки, значимое снижение отека периваскулярного пространства (рис. 3).
Было рекомендовано динамическое наблюдение, ведение дневника самоконтроля над астмой, продолжение биологической и базисной терапии.

Рисунок 3.
Капиллярные петли в виде шпильки, снижение отека периваскулярного пространства (увеличение × 400)
Figure 3.
Сapillary loops shaped as a “hairpin”, reduction of edema of the perivascular space (magnification × 400)
Обсуждение
Таким образом, в представленном клиническом наблюдении продемонстрирована перспективность практического применения метода компьютерной капилляроскопии ногтевого ложа в стационарных и амбулаторных условиях в качестве метода оценки гемодинамических нарушений при бронхиальной астме с целью верификации диагноза, проведения динамического наблюдения за сосудами на фоне лечения. Также показана эффективность проводимой генно-инженерной биологической терапии дупилумабом в течении тяжелой астмы в виде улучшения контроля над симптомами заболевания, улучшения показателей функции внешнего дыхания, а также положительного влияния на архитектонику сосудов микроциркуляторного русла.
Заключение
- Гетерогенность заболевания БА требует дифференцированного персонифицированного подхода к терапии в зависимости от эндотипа заболевания.
- Моноклональные антитела более 10 лет являются самыми эффективными препаратами для лечения тяжелой неконтролируемой бронхиальной астмы.
- Применение метода капилляроскопии ногтевого ложа имеет большое практическое значение в определении предикторов риска развития и течения заболевания, установления диагноза, а также оценки эффективности проводимой терапии.
Участие авторов / Author contribution
П.В. Бережанский — разработка концепции и дизайна исследования, редактирование, анализ полученных данных, общая ответственность.
А.Э. Хургаева — разработка концепции и дизайна исследования, сбор материала, обработка данных, подготовка текста, редактирование, анализ полученных данных, общая ответственность.
Т.А. Гутырчик — разработка концепции, обработка и анализ полученных данных, редактирование.
А.Б. Малахов — анализ полученных данных, редактирование.
С.И. Шаталина — анализ полученных данных, редактирование.
Н.Г. Колосова — анализ полученных данных, редактирование.
Pavel V. Berezhansky — conceptualization, data analysis, writing (reviewing and editing), overall responsibility.
Anastasia E. Khurgaeva — conceptualization, data collection, data processing, writing (the original draft, editing), analysis of the results, overall responsibility.
Tatyana A. Gutyrchik — conceptualization, data processing, analysis of the results, writing (reviewing and editing).
Alexander B. Malakhov — analysis of the results, writing (reviewing and editing).
Svetlana I. Shatalina — analysis of the results, writing (reviewing and editing).
Natalia G. Kolosova — analysis of the results, writing (reviewing and editing).
Список литературы
1. Global Initiative for Asthma Global strategy for asthma management and prevention, 2024. https://ginasthma.org/2024-report
2. Клинические рекомендации «Бронхиальная астма. Возрастная группа: дети/взрослые». 20.02.2024 г. (утверждено Минздравом России).
3. Gans M.D., Gavrilova Т. Understanding the immunology of asthma: Pathophysiology, biomarkers, and treatments for asthma endotypes. Paediatr Respir Rev. 2020;36:118–127. doi: 10.1016/j.prrv.2019.08.002.
4. Бережанский П.В., Гутырчик Т.А., Малахов А.Б., Коваленко И.В. и соавт. Особенности изменений в микроциркуляторном русле у детей с отягощенным аллергоанамнезом. Педиатрия. Consilium Medicum. 2022;4:344–348. doi: 10.26442/26586630.2022.4.202001.
5. Чумоватов Н.В., Захаров А.В., Черных Н.А., Романов В.В. Клинико-диагностические возможности капилляроскопии ногтевого ложа и перспективы применения метода во фтизиатрии и пульмонологии. Вестник Центрального научно-исследовательского института туберкулеза. 2024; 8(2):5–12.
6. Рывкин А.И., Андрианова Е.Н., Побединская Н.С., Решетова Т.Г. и соавт. Состояние микрогемоциркуляции при бронхиальной астме у детей. Педиатрия. Журн. им. Г.Н. Сперанского. 2006;85(6):7–11.
7. Ландышев Ю.С, Базилевич А.Ю, Чапленко Т.Н. Роль реопульмонографии в оценке эффективности базисной терапии при бронхиальной астме. Бюллетень физиологии и патологии дыхания. 2004;17:45–48.
8. Tavakol M.E., Fatemi A., Karbalaie A., et al. Nailfold capillaroscopy in rheumatic diseases: which parameters should be evaluated? Biomed. Res. Int. 2015;974530. doi: 10.1155/2015/974530.
9. Park H.S., Kim S.Y., Kim S.R. Targeting abnormal airway vascularity as a therapeutical strategy in asthma. Respirology. 2019;15(3):458–471. doi: 10.1111/j.1440-1843.2010.01724.x.
10. Крылова О.Ю., Пирогов А.Б., Колосов В.П. Артериоло-капиллярный кровоток в легких и легочная гипертензия у больных бронхиальной астмой. Пульмонология. 2009;3:71–74. doi: 10.18093/0869-0189-2009-3-71-74.
11. Petry D.G, Terreri М.Т, Len С.А. Nailfoldcapillaroscopy in children and adolescents. ActaReumatol. Port. 2008;33(4):395–400.
12. Бережанский П.В., Гутырчик Т.А., Мельникова И.М., Малахов А.Б. и соавт. Способ прогнозирования риска развития бронхиальной астмы у детей 7 лет и младше, имеющих отягощенный аллергологический анамнез. Патент на изобретение № 2789970, Российская Федерация, С1, МПК А61В 5/08.
13. Howell I., Howell A., Pavord I.D. Type 2 infl ammation and biological therapies in asthma: Targeted medicine taking fl ight. Experimental Medicine Division. 2023;7(220). doi: 10.1084/jem.20221212.
14. Геппе Н.А., Колосова Н.Г., Кондюрина Е.Г., Малахов А.Б., Мизерницкий Ю.Л., Ревякина В.А. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». 2017.
15. Schoettler N., Strek M.E. Recent Advances in Severe Asthma: From Phenotypes to Personalized Medicine. Chest. 2020;157(3):516–528. doi: 10.1016/j.chest.2019.10.009.
16. Авдеев С.Н., Ненашева Н.М., Жуденков К.В. Распространенность, заболеваемость, фенотипы и другие характеристики тяжелой бронхиальной астмы в Российской Федерации. Пульмонология. 2018;28(3):341–358. doi: 10.18093/0869-0189-2018-28-3-341-358.
17. Ивахненко И.В., Колесникова И.Ю. Тактика ведения пациентов с обострением бронхиальной астмы. Лекарственный вестник. 2020;14(4):20–28.
18. Kardas G., Kuna P., Panek M. Biological therapies of severe asthma and their possible effects on airway remodeling. Front.Immunol. 2020;11:1–11. doi: 10.3389/fimmu.2020.01134.
19. Sastre J., Dávila I. Dupilumab: a new paradigm for the treatment of allergic diseases. Journal of investig allergology and clinical immunology. 2018;28(3):139–150. doi: 10.18176/jiaci.0254.
20. Castro M., Corren J., Pavord I.D., Maspero J., Wenzel S., Rabe K.F., et al. Dupilumab Efficacy and Safety in Moderate-to-Severe Uncontrolled Asthma. New England journal of medicine. 2018;378(26):2486–2496. doi: 10.1056/NEJMoa1804092.
21. Ревякина В.А., Геппе Н.А. Практические рекомендации по применению биологических препаратов у сложных (коморбидных) больных с аллергическимм и аутоиммунными заболеваниями. г. Москва: «МедКом-Про», 2024.
Об авторах
П. А. БережанскийРоссия
Бережанский Павел Вячеславович, д.м.н., ведущий научный сотрудник отдела педиатрии; врач-педиатр пульмонологического отделения; профессор кафедры детских болезней клинического института детского здоровья имени Н.Ф. Филатова; доцент кафедры клинической иммунологии, аллергологии и адаптологии
ул. Коминтерна, 24а, стр. 1, г. Мытищи, 141009
4-й Добрынинский переулок, д. 1/9, г. Москва, 119049
ул. Большая Пироговская, д. 19, стр. 1, г. Москва, 119991
ул. Миклухо-Маклая, д. 6, г. Москва, 117198
А. Э. Хургаева
Россия
Хургаева Анастасия Эдуардовна, врач-педиатр
4-й Добрынинский переулок, д. 1/9, г. Москва, 119049
А. Б. Малахов
Россия
Малахов Александр Борисович, д.м.н., руководитель отдела педиатрии; врач-пульмонолог пульмонологического отделения; профессор кафедры детских болезней клинического детского здоровья имени Н.Ф. Филатова, главный внештатный детский специалист-пульмонолог Департамента здравоохранения г. Москвы и Минздрава Московской области
ул. Коминтерна, 24а, стр. 1, г. Мытищи, 141009
4-й Добрынинский переулок, д. 1/9, г. Москва, 119049
ул. Большая Пироговская, д. 19, стр. 1, г. Москва, 119991
Т. А. Гутырчик
Россия
Гутырчик Татьяна Александровна, врач-педиатр, врач-пульмонолог
4-й Добрынинский переулок, д. 1/9, г. Москва, 119049
С. И. Шаталина
Россия
Шаталина Светлана Игоревна, к.м.н., старший научный сотрудник; ассистент кафедры детских болезней клинического института детского здоровья имени Н.Ф. Филатова
ул. Коминтерна, 24а, стр. 1, г. Мытищи, 141009
ул. Большая Пироговская, д. 19, стр. 1, г. Москва, 119991
Н. Г. Колосова
Россия
Колосова Наталья Георгиевна, кандидат медицинских наук, доцент кафедры детских болезней клинического института детского здоровья имени Н.Ф. Филатова
ул. Большая Пироговская, д. 19, стр. 1, г. Москва, 119991
Рецензия
Для цитирования:
Бережанский П.А., Хургаева А.Э., Малахов А.Б., Гутырчик Т.А., Шаталина С.И., Колосова Н.Г. Применение метода капилляроскопии ногтевого ложа с целью оценки эффективности проводимой терапии (дупилумаб) у пациента с тяжелой бронхиальной астмой. Архив педиатрии и детской хирургии. 2025;3(2):58-65. https://doi.org/10.31146/2949-4664-apps-3-2-58-65
For citation:
Berezhanskiy P.V., Khurgaeva A.E., Malakhov A.B., Gutyrchik T.A., Shatalina S.I., Kolosova N.G. Using nailfold capillaroscopy to assess the effectiveness of ongoing therapy (dupilumab) in a patient with severe bronchial asthma. Archives of Pediatrics and Pediatric Surgery. 2025;3(2):58-65. (In Russ.) https://doi.org/10.31146/2949-4664-apps-3-2-58-65
JATS XML